Тогда попытайтесь дочитать до конца эту информацию, даже если она покажется вам скучноватой...
Помните из школы, что такое спирт? Это органическое соединение, в котором есть одна (или больше) гидроксильных групп (это пресловутый –ОН, вспомнили?..), напрямую связанных в молекуле с атомом углерода, причем атом этот должен быть насыщенным ( не иметь двойной связи... ). Самый простой пример, встречающийся в быту – этиловый спирт, или этанол, С2Н5ОН – кто же его не знает?...

Структурная формула этанола
Так вот, этанол содержит ОДНУ группу –ОН, это одноатомный спирт. А если формула будет выглядеть так?

Структурная формула глицерина
Получилась формула глицерина – трехатомного спирта (трехатомный – потому что содержит ТРИ группы –ОН). Глицерин и есть та «база», на основе которой строится практически ЛЮБОЙ жир.
Далее.
Органическая кислота – это органическое вещество, проявляющее свойства кислоты. Определено, что в формуле органической кислоты, на конце цепочки, присутствует так называемая «карбоксильная группа» - СООН, и остаток молекулы (иногда очень длинный...), который называется «радикал». Примером может служить всем известная уксусная кислота, формулу которой можно записать так СН3 – СООН, или, в развернутом виде:
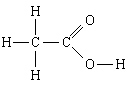
Структурная формула уксусной кислоты.
В уксусной кислоте -СН3 и есть «радикал» По этому принципу записывают и формулы других кислот:
C15H31 - COOH - пальмитиновая
C16H33 - COOH - маргариновая
C17H35 - COOH - стеариновая, и т.д.
Это НАСЫЩЕННЫЕ кислоты, то есть длинная цепочка атомов С (углерода) соединена ОДИНАРНОЙ связью, вот так:

Но существуют и НЕНАСЫЩЕННЫЕ кислоты, у которых цепочка атомов углерода местами соединена ДВОЙНОЙ связью, иногда в молекуле таких связей две, три или даже четыре. И тогда углеродная цепочка может выглядеть примерно так:

Можно отметить, что каждый атом С (углерода), к которому «подведена» двойная связь, удерживает только один атом Н (водорода), так как по одной валентности такие атомы С задействуют на образование этой самой двойной связи между собой. Упрощенно, валентность - это единица возможности образования связи с другим атомом. Обычно углерод четырехвалентен, а водород – одновалентен. Двойная связь является ненасыщенной, то есть способна быстро разрываться – и этом случае каждый из атомов С, между которыми была эта связь, может «прихватить» на свободную валентность атом водорода (если он будет «болтаться» где-то неподалеку...).
Примеры ненасыщенных кислот:
C15H29COOH – пальмитолеиновая (одна двойная связь);
C17H33COOH – олеиновая (одна двойная связь);
C17H31COOH – линолевая (две двойные связи);
C17H29COOH – линоленовая (три двойные связи);
C19H31COOH - арахидоновая (четыре двойные связи) – встречается редко...
Чтобы не путаться с длинными формулами и подсчетами атомов углерода и водорода в них, в общем случае принято записывать молекулу органической кислоты так:
R – СООН, где
R – этот самый «радикал», то есть цепочка атомов углерода, в которой могут быть и одинарные, и двойные связи – для каждой кислоты разный;
-СООН – верный признак органической кислоты – так называемая «карбоксильная группа».
А вот теперь перейдем к жирам.
Если к спирту добавить органическую кислоту, при определенных условиях произойдет следующая реакция (её называют реакцией этерификации...)
С2Н5ОН + СН3СООН —> СН3СООС2Н5 + Н2О, или словами
этанол + уксусная к-та = этиловый эфир уксусной к-ты + вода
Это частный случай реакции подобного типа. А если взять глицерин (трехатомный спирт) и три молекулы ЛЮБОЙ органической кислоты? Получим сложный эфир, образовавшийся в результате реакции глицерина и опять же ЛЮБОЙ из органических кислот!
CH2-OН| CH-ОН | CH2-OН + R¹-COOH + R²-COOH + R³-COOH = CH2-O-C(O)-R¹| CH-О-C(O)-R²| CH2-O-C(O)-R³ + 3 H2O,
где R¹, R² и R³ — радикалы (часто различных) жирных кислот.
или словами:
глицерин + орг.кислота 1 + орг.кислота 2 + орг.кислота 3 = триглицерид (ЖИР!..) + 3 молекулы воды
Это и есть этот самый «жир» (химическое название – триглицерид) - мы наконец-то до него добрались!
Благодарю вас - вы самоотверженно дочитали до этого места! Дальше будет чуть менее скучно...
Все разнообразие жиров основано на разнообразии остатков кислот, присоедившихся к глицерину. Очень часто это бывают три разные кислоты... Если «пристроились» только насыщенные кислоты – получаются твердые жиры, типа сливочного масла, сала, подкожного жира и т.д.. Как правило, это жиры животного происхождения. Если же с глицерином связаны ненасыщенные кислоты – появляются жидкие жиры, которые в обиходе обычно называют маслами. Природные масла добываются из растений: подсолнечника, рапса, хлопка, оливы...
В реальности любой твердый жир или масло – это достаточно разнообразная смесь триглицеридов с присоединившимися остатками различных органических кислот, как насыщенных, так ненасыщенных (с двойными связями...), причем в разных сочетаниях даже в одной молекуле жира. Их и разделить-то трудно...
В целом можно сказать, что чем больше степень насыщенности «радикала» – тем тверже жир, тем выше температура его плавления, тем сложнее усвоить его человеческому организму и тем меньше от него толку – а часто как раз наоборот – больше вреда... Соответственно – чем более ненасыщенными являются кислоты, входящие в состав жира, тем более текучий, жидкий жир мы имеем, тем легче он перерабатывается организмом и больше полезных свойств проявляет...
Сейчас мы с вами добрались только до понимания : что же это такое - ЖИР! Огромный массив данных о различных жирах – свойства, характеристики, роль в организме (причем одна из важнейших - энергетическая!.. Расщепление одного грамма жира в организме дает 9 килокалорий – вдвое больше, чем углеводы и белки!), получение, применение в быту и т.д. – остался, к сожалению, неосвещенным. Но фундаментальное понятие о жире, о его строении, у всех, кто умудрился дочитать до конца, несмотря на непреодолимую сонливость и зевоту – есть!